2.2.4. ЦИКЛИЧЕСКИЕ 3’, 5-НУКЛЕОТИДЫ И ИММУНОСТИМУЛЯЦИЯ РОСТА ОПУХОЛИ
Циклические пуриновые нуклеотиды — цАМФ и цГМФ — играют важную физиологическую роль практически во всех видах обмена веществ в клетке в их фенотипическом проявлении. Помимо этот, имеются прямые указания на участке аденилатциклазной системы в контроле механизмов генетической информации за счет изменения активности ферментов, регулирующих ijx к фо-
рилирование гистонов.
Обнаружено также участие цАМФ в формировании иммунного ответа и механизмах фагоцитоза. Установлена роль цАМФ и зависимого от цАМФ фосфорилирования белков в низкоспециализированных клетках (фибробласты и др.) в отличие от таковой в лимфоцитах и подобных им высокоспециализированных клетках в поддержании состояния покоя и жизнеспособности этих покоящихся клеток, а также в поді^товкс их компетентности к пролиферативному ответу. Следовательно, многообразие физиологическою действия цАМФ реализуется на молекулярном, клеточном и организменном уровняхХотя функции цГМФ исследованы мало, полагают, что этот нуклеотид является антагонистом цАМФ, выполняющего роль универсального регулятора репликации, транскрипции, трансляции, активности многих ферментов, регулятора размножения клеток и экстрацеллюлярною передатчика («сигнал»- молекула) специфических стимулов и информации от одних типов клеток к другим. Считают, что если цАМФ является стоп-сигналом пролиферации и одновременно пусковым сишалом дифференцировки, то цГМФ тормозит эти процессы. Однако имеются сведения о том, что цАМФ может в одних случаях функционировать как переносчик стимулирующих пролиферацию сигналов, а в других — как переносчик ингибирующих сигналов Существенное значение определенною уровня цАМФ в сохранении специфической дифференцировки было показано на различных опухолевых и трансформированных клетках, которые восстанавливали исходную дифференцировку при увеличении концентрации цАМФ внутри клетки. В то же время неопластическая трансформация практически всегда сопровождается статистически достоверным снижением содержания цАМФ и явно выраженным дефектом аденилатциклазы, фосфодиэстеразы, цАМФ-зависимых протсинкиназ, транспорта Са2* и т.
д. Следовательно, есть основания полагать, что тесно взаимосвязанная система циклические 3', 5’ -нуклеотиды — внутриклеточный Са2* является одним из основных регуляторных механизмов, обусловливающих процессы дифференцировки и неопластической трансформации {Агеенко А. И., 1978; Федоров Н. А., 1979; Кравцова Т. Н., Агеенко А. И., 1983; Епифанова О. И. и др., 1988; Johnson G. S., 1975; Rasmussen С. D., 1982].В экспериментах на us-мутантах онковирусов выявлена прямая корреляция между внутриклеточным уровнем цАМФ и некоторыми свойствами трансформированных клеток, такими как адгезивность,морфология, нечувствительность к межклеточным контактам, увеличение агглютинируемое™ под действием растительных лектинов и др. Более злокачественные клетки характеризуются низким содержанием цАМФ и большей чувствительностью к воздействию экзогенною цАМФ или же вещества, индуцирующею ею внутриклеточный синтез. Добавление дибутирил-цАМФ и экзогенною цАМФ ингибирует рост злокачественно трансформированных клеток in vivo и in vitro, а также восстанавливает их морфологические и функциональные свойства {Кавсцкий Р. Е., 1977].
Получены противоречивые данные об индукции экспрессии «ранних» генов (fos и myc) пролиферативною ответа под воздействием цАМФ. Установлено, что влияние цАМФ на экспрессию протоонкогенов myc и fos зависит как от типа клеток, так и особенностей действия митогена. Вероятнее всею, клетки, проходящие пререплякативный период, нуждаются в двухфазном изменении концентрации цАМФ. Иными словами, согласно представлениям некоторых исследователей, стимулирующеевоздействие цАМФ на синтез ДНК
ограничено ранними пролиферативными событиями, а в последующем такие клетки требуют снижения уровня цАМФ [Olashaw N. Е. ct al., 1984; Rah W. et al., 1986}. По мнению W. Kan и соавт, (1986), экспрессия протоонкогенов lbs и myc может регулироваться под контролем ЭФР с использованием Са2* и цАМФ в качестве кооперирующих цитоплазматических переносчиков.
S. Manam и соавт.
(1989) представили данные, позволяющие предполагать, что изменение обмена фосфолипидов, Са2* и активности протеинкиназы С (увеличение) может быть основным компонентом пути, который приводит к быстрой ранней экспрессии протоонкогенов с-тус и c-fos. В отличие от этого цАМФ может играть существенную роль в пролонгированной индукции c-fos под действием сыворотки и поздней экспрессии с-тус в процессе двухфазной стимуляции под действием различных ФР.В дальнейшем при развитии пролиферативного процесса с включением «поздних» генов пролиферативного ответа (семейство ras) увеличение внутриклеточного содержания цАМФ сначала приводит к активации протоонкогена ras, а затем к снижению экспрессии этого гена, как полагают, в результате посттранскрипционной регуляции [Chiarugi V. ct al., 1985; Blomhoff Н. К. etal., 1987; Franks D. J. etal., 1987; Spina A. et al., 1987}. Следовательно, цАМФ в культивируемых и в неспециализированных клетках регулирует их размножение, выполняя функцию как ингибитора пролиферации, так и стимулятора данного процесса. Это происходит вследствие увеличения чувствительности покоящихся клеток к ФР и изменения экспрессии протоонкогенов пролиферативного ответа, предшествующего синтезу ДНК и митозу. .
В неопластически трансформированных клетках стимуляция их размножения онкобелком р21гм приводит к увеличению концентрации цАМФ в раннем пререпликативном периоде [Franks D. Y. et al., 1985]. В то же время добавление экзогенною цАМФ, вызывающее реверсию трансформированною состояния клеток NIH/3T3, не изменяет повышенной экспрессии онкогена ras. Это свидетельствует об участии цАМФ в процессах, непосредственно нс зависящих от функции данного гена [Ridgway A. G. et al., 1988}. При обосновании механизма опухолевой трансформации клеток щитовидной железы с участием цАМФ была отмечена избирательная активация каскада цАМФ, характеризовавшегося ранней и преходящей экспрессией протоонкогена с-тус [Маеп- haut С. ct al., 1991 ]. . ..
Итак, на многих тест-системах установлено, чтонеопластически трансформированные клетки имеют низкий внутриклеточный уровень цАМФ, который не зависит от плотности клеток.
Дело в том, что в культурах нормальных клеток, когда их плотность становится критической, они прекращают деление и уровень цАМФ резко возрастает, т. е. происходит контактное ингибирование роста. Трансформированные же клетки, наоборот, при высокой клеточной плотности продолжают деление, и уровень цАМФ при этом остается таким же или еще больше снижается [Johnson G. S., 1975].Вместе с тем во многих быстрорастущих неоплазмах, наоборот, иногда определяется высокое содержащие цАМФ и при повышенном уровне цАМФ стимулируется синтез ДНК. Вероятно, такие противоречивые данные можно объяснить сложностью взаимосвязей в этой регуляторной системе клетки. Очевидно, цАМФ активирует фосфорилирование регуляторных и структурных клеточных белков. Предполагают, что морфологическая нормализация трансформированных клеток цАМФ обусловлена его действием на активность поверхностных гликозилтрансфераз. Таким образом, большая совокупность
признаков воздействия цАМФ, характеризующих трансформированный фх?- нотип.клеток in vitro, находится под контролем цАМФ Подучены менее убедительные данные, свидетельствующие о влиянии цАМФ на процессы дифференцировки, так как наблюдались и повышение, и снижение дифференцировки при воздействии цАМФ на клетки. Анализ исследовании, посвященных изучению участия протоонкогена туе (с учетом концентрации цАМФ) на разных этапах дифференцировки, позволяет прийти к заключению о том. что, вероятно, только на одном этапе (предшествующем терминальной дифференцировке) необходимо изменение экспрессии этою ієна и, по-видимому, про- тгонкогена fos. Возможно, этим и объясняются противоречивые данные об участии цАМФ в дифференцировке |Lomo J. et al., 19X7; Nepven A et al., 19X7; Tsuda H. et al., 19X7; Connoly J. A. ct al., 19X8; Freytag S. 0., 19XX|.
Внутриклеточная концентрация цАМФ зависит от взаимодействия нескольких факторов: активности аденилатцикдазы, локализованной на поверхности клеточной мембраны и регулируемой гормонами; скорости деградации под действием фосфодиэстсразы (цАМФ может активировать синтез этою фермента) и выхода цАМФ в межклеточное пространство.
В клетках хлокачсственных новообразований нарушается, как полагают, взаимодействие аленилатцикла- зы с мембраной, что приводит к снижению базальною уровня цАМФ. Получены данные, согласно которым аленилатниклаза трансформированных клеток утрачивает способность активироваться гормонами, специфичными для этих клеток (Chlapowski F. J. et al., ,975).В экспериментах на многих тест-системах обнаружено, что в нсопдасти- чсски трансформированных клетках внутриклеточная концентрация цАМФ обычно в 2—К) раз меньше, чем в соответствующих нормальных прототипах. Показано, что в нредлейкозном периоде у мышей активность адснилатцикла- зы и уровень цАМФ даже несколько повышаются (Mcnahan L. A ., Kemp R. G., 1976). Однако на более поздних этапах лсйкозоіснсза содержание цАМФ снижается вследствие резкою увеличения (в 2—4 раза) активности фэосфэодиэстс- разы. Очевидно, снижение уровня внутриклеточного цАМФ в клетках пока- чественнмх новообразований обусловлено, вероятнее всею, ускоренным размножением клеток, а нс переключением их на путь автоматизации. Аналогичная картина, как известно, наблюдается при стимуляции пролиферации культур клеток путем добавления свежей сыворотки, тогда как с увеличением насыщенности культур в стационарной фазе роста концентрация цАМФ возрастает. Следует обратить внимание на то, что в некоторых случаях были получены разноречивые результаты, если авторы этих экспериментов нс учитывали специфику используемой сыворотки, а также нспролифюрируюшис клетки в трансформированных культурах. При этом необходимо помнить, что метаболические характеристики нормальных и трансформированных покоящихся клеток различны (Gionti Е., Lawrence D. А., 1977; Nico,ini С., Belmont А., 19821- Важно отмстить, что разработано мною разных критериев, позволяющих идентифицировать покоящиеся нормальные и неопластически трансформированные клетки (Wallen С. A. ct al., 1984; Tolsma S. S. et al., 19X8).
Наиболее низкое содержание цАМФ отмечено в период митоза, причем в нормальных клетках этот показатель уменьшается в большей степени, чем в трансформированных клетках.
Непосредственное действие цАМФ в качестве сигнала к делению в момент снижения уровня этою нуклеотида доказывается снятием стимулирующею митоз эффюкта при действии протеаз или сыворотки в результате добавления дибутирил-цАМФ, но только в течение 3 мин пос-;ic обработки протеазами. Вместе с тем пока неясно, действительно ли во всех случаях изменение поверхности плазматических мембран приводні к изменению концентрации цАМФ. Нс учтено также, ассоциировано ли снижение внутриклеточноп) уровня цАМФ с аденилатцнклазой или фосфод и эстеразой или является следствием более интенсивной утилизации цАМФ в процессе митоза. Наконец, нс выяснен принципиальный вопрос, является ли изменение концентрации единственным или основным связывающим фактором между поверхностной мембраной и ядром клетки. Предполагают, что значительное снижение содержания внутриклеточного цАМФ в период фаз S и М клеточного цикла является следствием возрастающей активное ги фосфодиэстеразы в эти периоды по сравнению с таковым вфазе G,. С помощью дибутирил-цАМФ доказывается пусковая роль критической внутриклеточной концентрации цАМФ в переходе клеток из фазы G, в митоз. После добавления дибутирил- цАМФ наблюдалась задержка пика митозов без изменения синтеза ДНК, в то время как удаление дибутирил-цАМФ из среды в конце фазы S, наоборот, ускоряло пик митозов. На этом основании предполагают, что цАМФ регулирует клеточный цикл, влияя на процесс митоза.
Возможно, что и неопластическая трансформация клеток также связана с изменением в системе аденилатциклаза— фосфодиэстсраза цАМФ, рейдирующей уровень внутриклеточноп) цАМФ. Поскольку цАМФ, очевидно, инициирует деление клеток, можно предполагать, что в трансформированных клетках из-за нарушения функционального контакта между ними это действие цАМФ «выпадает» вследствие неспособности клеток либо войти в соответствующий физико-химический контакт, либо образовать достаточную кон- цен грацию цАМФ, или в результате нарушения связи между инициированием фазы S и цАМФ, или, наконец, наступления этой фазы при концентрации цАМФ более высокой, чем в нормальных клетках. Следует подчеркнуть, что в быстрорастущих нормальных клетках уровень цАМФ значигслыю меньше, чем в медленно растущих. Остановка роста клсюк в культуре сопровождается резким увеличением концентрации цАМФ. Этою свойства полностью лишены злокачественно трансформированные клетки, в чем, по-видимому, заключается основной дефект реіуляции их роста. Правда, пока неясно, какой механизм обеспечивает постоянно низкий внутриклеточный уровень цАМФ и делает ею независимым от воздействия окружающей среды.
Активность аденилатциклазы в трансформированных клетках значительно понижена, что нарушает синтез цАМФ из АТФ. Адени ла і циклаза локализуется в плазматических мембранах, структуры и функции которых наиболее сильно изменены в неопластичсски трансформированных клетках. В то же время активность фосфодиэстарсза цАМФ в таких клетках нс отличается от нормы. Следовательно, грансформированныс клетки способны поддерживал, раснал цАМФ на уровне, свойственном нормальным клеткам. Таким образом, нарушения согласованной деятельности двух основных і])ермеіттов метаболизма цАМФ в процессе опухолевой трансформации лежат в основе глубоких изменений обмена этою универсального реіулятора клеточных функций.
Проведено сравнительное исследование влияния іуанилатниклазы, ^юсфо- диэстсразы цГМФ и уровня цГМФ на параметры пролиферации в нормальных и трансформированных фибробластах в культуре INesbiu J. A. et al., 1976]. Стимулирование іуанилатциклазьі под действием ФР фибробласт»» не обнаружено. Активності, этого фермента низкая в гсченис фазы лоїарифмичсскою роста и возрастает при замедлении росла с увеличением насыщенности кулыур.
В клетках, трансформированных Ki-MSV, активность іуанилатциклазы нс проявлялась. Трансформация клеток почки крысы Ki-MSV, Ha-MSV и RSV (штамм Шмидта-Руппина) приводит к снижению активности фермента в клетках. После трансформации фибробластов BALB/3T3 онкорнавирусами (Мо- MSV, Ha-MSV и Ki-MSV) или SV40, мстил Хол антреном или после спонтанной трансформации активность гуанилатциклазы также уменьшается, но ее еще можно измерить. Активность фосфодиэстеразы цГМФ несколько возрастает при вступлении клеток в стационарную фазу. В двух клонах почечных клеток крысы, трансформированных Ki-MSV, активность этот фермента не выявлялась и снижалась в третьем клоне клеток. Трансформация почечных клеток Mo-MSV и RSV почти не влияет на активность фосфодиэстеразы. Обнаружено, что снижение этого показателя в процессе грансформации нс было вызвано потерей активатора указанного фермента. Уровень цГМФ в трансформированных онковирусами клетках почки крысы оказался значительно ниже, чем в нормальных клетках в насыщенной культуре. Это связано со значительным снижением активности гуанилатциклазы после трансформации клеток. Следовательно, представленные факты не согласуются с мнением о том, что цГМФ способствует росту фибробластоподобных клеток;
Участие цАМФ в неопластическом превращении клеток в последнее время связывают с функционированием микроканальцевых структур — характерного фиброзного каркаса клеток эукариотов. Основными функциями микроканал ьцев является обеспечение формы клетки и клеточной поверхности, движения хромосом при митозе, внутриклеточною транспорта. Установлено, что эти функции контролируются цАМФ. Тубулинмономсрная единица микроканальцевых элементов служит субстратом для цАМФ-зависимой протеинкиназы. Препараты тубулина обладают киназной активностью, стимулируемой цАМФ. В частности, обнаружено, что антимитотический алкалоид винблас- тин, связывающийся с тубулином, блокирует антипролиферирующий эффект цАМФ в * трансформированных клетках.
Выше отмечалось, что взаимосвязанная система циклических нуклеотидов — Са** опосредует нс только регуляцию роста клеток и их дифференцировку, но и иммуногенез, и функциональное состояние иммунокомпетентных клеток. Известно, что биологические эффекты циклических нуклеотидов в первую очередь определяются их концентрацией и перераспределением Са2* в клетке, являющеюся одним из основных посредников в передаче митогенною сигнала через мембрану лимфоцита |Hart D. А., 1981; Rasmussen Н. et al., 1982; Toyoshima S. ct al., 1982; Lichtman A. H. et al., 1983]. Установлено, что увеличение концентрации цГМФ после взаимодействия лимфоцита с внеклеточным сигналом происходит в результате не прямой активации фермента этим сигналом, а активации цитозольной гуанилатциклазы Са2* [Hardman J. G. et al., 1971J. Показано, что при бластом атозном процессе, как правило, имеет место изменение активности таких мембранно-связанных ферментов лимфоцитов, как аденилатциклаза, фосфодиэстераза и АТФ аза [Hardman J. G. et al., 1971; Ellegard I. ct al., 1975]. Первые два фермента, как отмечалось, обусловливают внутриклеточный уровень циклических нуклеотидов (цАМФ и цГМФ), а АТФаза способствует изменению электролитною баланса, в том числе и кальциевою, играющего важную роль при запуске механизмов, которые обеспечивают стимуляцию лимфоцитов [Ellegard 1. et al., 1975; Freedman M. N., 1979].
А. И. Агеенко иТ,Н. Кравцова (1982, 1983, 1985) исследовали уровень цАМФ и цГМФ;-АТФазную активность, транспорт Са2* в лимфоцитах пери-
Рис 17 Содержание цАМФ (а) и цГМФ (б) в лимфоцитах хомяков.
I - содержание в норме, 2 • в контроле с трансплантацией клеток нормальных органов. 3 • в опыте с опухолью Rapp HSV2. По оси ординат • концентрация циклических нуклеотидов (пмоль на 1(Р клеток).
фсрической крови и лимфатических узлов. Определяли трансмембранный потенциал их плазматической мембраны в процессе аденовирусного канцерогенеза (сирийские хомяки + вирус SA7(C8)J и при росте у хомяков перевивной опухоли RappHSV2, вызванной фибробластами, трансформированными вирусом простого герпеса типа 2 (фибробласты вводили в защечный мешок).
Оказалось, что у хомяков с перевивной опухолью содержание цАМФ в лимфоцитах в 1,5—2 раза выше, а уровень цГМФ в 2,2 раза ниже, чем в контроле (рис. 17). Соответственно этим изменениям модифицировалось отношение цАМФ:цГМФ. У нормальных животных оно составляло 8,3, а у хомяков с перевивной опухолью — 3,2. Следует отметить, что концентрация циклических нуклеотидов в лимфоцитах хомяков, которым вводилась взвесь клеток нормальных органов, не отличалась от контроля. Таким образом, изменения концентрации циклических нуклеотидов в лимфоцитах происходят только тогда, когда животным перевивают опухоль, и не зависят от антигенных различий. Оказалось, что в лимфоцитах хомяков как общая АТФазная активность (в 1,7 раза), так и активность Na*-, К*-зависимой АТФазы (на 60%) и Са^-зависимой АТФазы (на 40%) выше у животных с перевивными опухолями. Аналогичные сдвиги активности АТФаз (зависимых от Na*, К*. Mg2* и Са2* имелись в лимфоцитах и тимоцитах хомяков в период прогрессивного роста опухолей (30, 40 и 50-й день после появления опухолевого узла), индуцированных вирусом SA7(C8). Если же хомякам вводили клетки нормальных органов, то такою повышения АТФазной активности нс наблюдалось.
Известно, что транспорт Са2* является одним из основных механизмов активации иммунокомпетентных клеток. Вполне очевидно, что обнаруженные нами изменения в концентрации цАМФ и цГМФ в лимфоцитах животных в период прогрессивного роста перевивных и вирусиндуцированных опухолей оказывают определенные воздействия на перераспределение в них Са2*. Действительно, у животных-опухолсносителей КонА нс увеличивал поглощение Са2* лимфоцитами периферической крови и даже немного снижал транспорт Са2* в лимфоциты лимфатических узлов. В то же время КонА увеличивал более чем в 2 раза транспорт Са2* в лимфоциты периферической крови и лимфатических узлов хомяков обеих контрольных групп (рис. 18).
Исследование кинетики поглощения Са2* лимфоцитами показало, что под действием КонА этот процесс у животных-опухолсносителей не активируется во времени (рис. 19). К 15-й минуте поглощение Са2* достигало максимума, равного поглощению Са2* без митогена. В обеих контрольных группах, наоборот, под действием КонА происходило увеличение поглощения Са2* лимфоцитами, развивающееся во времени и достигающее максимальных значении к 60-й минуте инкубации (см. рис. 19). С помощью реакции бласттрансформа- ции было установлено, что активность лимфоцитов лимфатических узлов хо- мяков-опухоленосителей по отношению к КонА понижена, тогда как индексы стимуляции лимфоцитов узлов контрольных животных обеих групп практически не отличались.
159

б

І’мс. JK. Нлияние КонА на поглощение кальция лимфоцитами периферической крови (а) и лимфатических углов (б) хомяков. I • контроль; 2 • контроль е трансплантацией меток нормальных органов; .< • опухоленосители; А • бег КонА. И - с КонА. По оси ординат - концентрация 4'Са в пмоль на 1(Р (а) и НУ (б) клеток.
Рис. 19. Кинетика поглощения 4'Са лимфоцитами лимфатических углов хомяков в отсутствие и при добавлении КонА.
/ - контроль плюс КонА; 2 - контроль с трансплантацией клеток нормальных органов плюс КонА; - контроль бег митогена. 4 • контроль бег митогена. < -лимфоциты животных-оп\ко- ясное ителсй плюс КонА: б ■ то же бег митогена. По оси абсциі е - время (мин). По оси ординат • концентрация * Со Iпмоль на НУ меток).

Итак, у хомяков-онухолсноситслсй копошение Са2* лимфоцитами нс активировалось КонА, оставаясь на уровне контроля, а их реактивность, оценивая в реакции бласттрансформании, 6i.lt а снижена. Одновременно в этих же иммунокомпетентных клетках изменялось соотношение цАМФдіГМФ. Нельзя ИСКЛЮЧИТЬ, что резкое повышение уровня цАМФ в лимфоцитах и понижение копнен грации цГМФ препятствовали ак і икании КонА транспорта Са2* в эги к. їстки, поскольку известно, что цГМФ (К) 'М) может усиливать транспорт Са4, индуцированный КонА, а дибутирил-нА МФ (К)2—1()4М) ингибирует этот процесс (Freedman М. N et al., 1975J. Помимо этою повышенная, активность Са2*-зависимой АТФазы в лимфоцитах хомяков-онухолсноситслсй, вероятно, поддерживает низкую внутриклеточную концентрацию Са'4. Таким образом.
совершенно очевидно, что у животных с прогрессивным ростом опухоли нарушена одна из первичных биохимических сіадий, приводящих к активации лимфоцитов, а следовательно, и к митогенезу, индукция транспорта Са2* в лимфоциты | Кравцова Т. Н., Агеенко А. И., 1983J.
Эги факты, свидетельствующие о нарушении первичных стадий активации иммунокомпетентных клеток при опухолевом росте, были подтверждены также нами при исследовании трансмембранного потенциала тимоцитов интактных хомяков и хомяков-опухоленосителей. Оказалось, что мембрана лимфоцитов животных с прогрессивным ростом опухоли гиперполяризована несколько больше, чем мембрана нормальных тимоцитов (рис 20, 21). Известно, что изменение трансмембранною потенциала лимфоцитов играет существенную роль при передаче митогенною стимула [Gerson D. F., Kiefer Н., 19К1 ]. Иными словами, эпектричсский потенциал плазматической мембраны иммунокомпетентных клеток наряду с изменениями соотношения цАМФ:цГМФ и транспорта Са2* также является одним из первичных факторов, обусловливающих функциональную активность лимфоцитов. Следовательно, изменение всех перечисленных выше параметров физиологических реакций иммунокомпетентных клеток у животных-опухолсносителей СВИДСТСЛЬСТВуСТ о нарушении у них первичной стадии активации

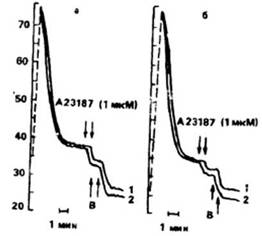
Рис. 20. Влияние валиномицина (В), грамицидина (Г) и КС1 на флюоресценцию ilis-CrfS) в t успетии тимоцитов интактных хомяков (а) и хомяков-опухоленосителей (б).
в - калибровочная кривая. По оси ординат - интенсивность флюоресценции (отн. ед.). Кривые - объяснение см. в тексте.
Рис. 21. Флюоресценция dn-Cf-(5) в суспензии тимоцитов интактных хомяков (а) и хомяков-опухоленосителей (б)
В • валиномицин ! - контроль- 2 - опыт Среда инкубации содержала / мМ 'дГТА (а) или I иМ Са2' (б) По оси ординат - то же, что на рис. 20
X 1—173
ш
В последующей серии экспериментов бьиа предпринята попытка исследовать роль і ~»МФ в усилении роста опухоли, опосредованном лимфоцитами сингенных животных, с целью выявления общих механизмов стимуляции независимо O'[IV]- природы индуктора [ Агеенко А И и др , 1978]
На основании анализа приведенных выше работ можно сделать вывод о том, ч го обратная зависимость между внутриклеточным содержанием цАМФ и уровнем митотической активности является универсальной закономерностью нормальною и опухолевою фенотипов Вместе с тем этот вывод следует принимать с осторожностью, поскольку в оценке роли цАМФ в регуляции пролиферативной активности нсопластически трансформированных клеток существует ряд трудностей, основная из которых состоит в выборе нормального юмолога для установления исходною уровня цАМФ Совершенно очевидно, что для решения этою вопроса необходима адекватная система с использованием определенною типа опухолевых клеток, нос заведомо разными темпами роста стимулированным и обычным Исходя из этого, бьиа изучена кинетика роста к определено содержание внутриклеточного цАМФ клеток одного типа опухоли SA7(C8)-capKOM, вызванных у мышей линии СВА аденовирусом обезьяны SA7(C8), с ускоренным и обычным темпом роста Как и в ранее описанных экспериментах, рост опухоли стимулировали неиммунными сингенными спленоцитами в соотношении 1 10 Критерием оценки темпов роста опухоли служил индекс массы опухоли, который вычислялся в динамике роста сарком на 10-, 20- и 30-й день В эти же сроки канцерогенеза определяли'в клетках этих же сарком внутриклеточное содержание цАМФ (рис 22, 23)
Как видно из рис 22, имеется линейное нарастание массы опухоли, клетки которой вводили сублетально облученным животным в смеси с неиммунными сингенными спленоцитами в соотношении I К) Темпы роста опухоли, тестируемые по динамике изменения массы, возрастают к 20- му дню с момента их возникновения и снижаются по сравнению с контролем в период от 20-го до 30-го дня носительства но

рме 22 Кинетика роста саркомы SA7(C8)
1 - опухоль, стимулированная нормальными лимфоцитами в соотношении / 10 2 - опухоль не стимулированная нормальными лимфоцитами По оси абсцисс - время (дни) По оси ординат - масса опухоли (г)
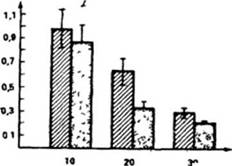
Рис 23 Внутриклеточное содержание цАМФ на разных стадиях канцерогенеза SA7 (С8)
эо
вообразований при сохранении различий по абсолютной массе (13,6 г в группе с ускоренным ростом против 12,1 г в контроле, р>0,05). Возможно, сближение темпов роста сарком в экспериментальной и контрольной группах за счет ускорения их роста в контроле свидетельствует о том, что увеличение массы опухолей с определенного этапа их развития — в значительной мере процесс автоматический, зависящий от накопления «критической массы» опухолевых клеток. Достижение этой массы саркомами, обработанными спленоцитами, происходило быстрее, чем в контроле. Следовательно, можно сделать вывод, что факторы, обусловливающие ускорение роста опухоли в исследованной системе, действуют в течение длительного времени (сокращение сроков латентного периода и нарастание темпов увеличения массы опухолей до 20-го дня), после чего вступают в силу другие факторы, определяющие кинетику роста SA7(C8)-capKOM.
К сожалению, в рамках данного эксперимента нельзя ответить на вопрос, в какой степени ускорение роста опухоли в исследованной системе вызвано наследуемыми изменениями неопластически трансформированных клеток, учитывая, что опухоль представляет собой систему взаимодействующих субпопуляций с исходно различными свойствами. Однако в любом случае из представленных экспериментов следует, что при определенных условиях взаимодействие опухолевых клеток с популяцией клеток интактной селезенки может быть существенным фактором опухолевой прогрессии.
Обнаруженная корреляция (см. рис. 23) между внутриклеточным содержанием цАМФ и темпами роста опухоли указывает на то, что использованный в данной работе биологический индуктор ускорения роста опухоли (нормальные спленоциты) не обладает какими-либо отличиями в регуляции пролиферации клеток сарком (определяется концентрацией цАМФ). Это, естественно, тем самым подчеркивает универсальность роли данного нуклеотида в обеспечении клеточной пролиферации. Иными словами, четко показана обратная зависимость между темпами роста SA7(C8)-capKOM, стимулированных спленоцитами от интактных сингенных мышей, и уровнем внутриклеточного цАМФ. При этом следует подчеркнуть, что использование в описанных экспериментах одного типа клеток опухоли с заведомо разными темпами роста позволяет связать изменения в концентрации внутриклеточного цАМФ с усилением их пролиферативной активности. Эго особенно важно, если учесть, что вариации содержания цАМФ в опухолевых клетках от нормальной) до повышенного и пониженной) уровней (см. выше) могут отражать главным образом не только изменения ростовых потенций опухоли, но и особенности метаболизма клеток различных типов злокачественных новообразований.
Представлена математическая модель иммуностимудяции роста опухоли (Агеенко А. И., Вериго В. В., 1987]. Показана принципиальная возможность существования нетривиальною стационарною решения модели, соответствующего временной стабилизации роста опухоли при стабилизации популяций лимфоцитов — эффекторов и супрессоров. Устойчивость этою решения оценивается по линейному приближению с помощью известных неравенств, вытекающих из критерия Рауса — Гурвица (Айзерман М. А., 1958], и при возможности идентификации всех структурных параметров модели она может быть оценена для конкретной экспериментальной ситуации.
Значительные упрощения, сделанные при составлении модели, требуют относиться к полученному результату с определенной осторожностью. Однако он может служить дополнительным аргументом в пользу существования эффекта иммуностимудяции роста опухоли, а также иллюстрирует целесообразна
ность применения метода математическою моделирования при исследовании динамики t .южных биологических процессов.
Еще по теме 2.2.4. ЦИКЛИЧЕСКИЕ 3’, 5-НУКЛЕОТИДЫ И ИММУНОСТИМУЛЯЦИЯ РОСТА ОПУХОЛИ:
- 2.1.4. Сравнение темпов роста доходов СЭО в сравнении с темпами роста средней заработной платы населения и инфляции.
- Типы экономического роста. Оценка роли факторов предложения в формировании экономического роста
- Эволюция подходов и сущность экономического роста. Типы экономического роста
- 9.4.1. Циклические изменения
- Циклическая безработица
- Циклические, или периодические, изменения.
- Интонация циклической нецелесообразной деятельности
- Циклический тип социальных изменений.
- Опухоли околоушной железы
- § 3. Возникновение и развитие плюрально-циклических концепций истории
- Циклическое отношение к Политическому
- Биологические и фенотипические особенности опухолей